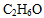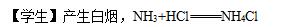化学用一套共同的符号和标记体系来描述和表示物质,例如化学式、反应方程式和化学结构式等,简化了科学交流和研究。这里给大家分享一些关于中考名师初中化学教案,供大家参考学习。

中考名师初中化学教案【篇1】
一、教学目标
(一)知识与技能
1.知道化学是在分子、原子层次上研究物质的性质、组成、结构与变化规律的科学。
2.知道化学与人类进步和社会发展关系密切。
(二)过程与方法
1.通过具体的事例,体会化学与人类进步及社会发展的密切关系,认识学习化学的价值。
2.通过小组合作学习、讨论交流,培养良好的学习习惯和学习方法。
(三)情感、态度与价值观
2.激发学生对化学的兴趣和探究的欲望。
1.激发学生对化学的兴趣和探究的欲望。
三、教学难点
知道化学是在分子、原子层次上研究物质的性质、组成、结构与变化规律的科学。
四、教学准备
实验用品:事先用酚酞溶液写好“化学”字样并晾干的滤纸,事先用酚酞溶液画好“小笑脸”并晾干的滤纸,稀氢氧化钠溶液,稀盐酸,浓氨水。
中考名师初中化学教案【篇2】
教学目标:
1.感受化学在促进社会发展和提高人类生活质量方面的重要作用,初步树立为民族振兴、为社会进步学习的志向。
2.认识物理变化、化学变化的基本特征,激发对化学现象的好奇心和探究欲,提高学习化学的兴趣。
3.知道物质是由分子、原子等粒子构成的,初步形成物质构成的微粒观。
4.初步建立宏观与微观联系的思维方式。
5.认识化学的两面性,初步树立绿色化学观。
重点、难点:
1.认识物理变化、化学变化的基本特征。
2.知道物质是由分子、原子等粒子构成的,初步形成物质构成的微粒观。
3.初步树立为民族振兴、为社会进步学习的志向。
教学过程:
[创设情景]在我们正式学习化学课前,请同学们谈谈你在生活中所感知的与化学有关的知识和经验。
一、化学给我们带来了什么?
[提出问题]化学给我们带来了什么?
[学生活动]设想来到与世隔绝的荒岛,没有了化学制品,你的生活会是什么样子?
二、观察化学变化
[活动天地]观察化学变化的现象。
引导观察现象,认识仪器,准确地记录并记忆实验现象。部分环节由学生参与完成,活跃课堂气氛。
总结以下几点:
1.化学变化的基本特征。
2.化学变化与物理变化的区别。
3.开展化学研究的基本目的。
4.认识化学的两面性,了解绿色化学观。
三、化学变化的奥秘
阅读想象水的构成,初步建立宏观与微观联系的思维方式。明确以下几点:
1.水是由大量的水分子构成的。
2.每个水分子由一个氧原子和两个氢原子构成。
3.水分子是保持水的化学性质的最小粒子。
4.化学变化的本质就是生成了与原来物质组成或结构不同的新物质。
5.通过原子种类、元素种类、物质种类的数量比较,体验物质构成的丰富多彩。
[课堂小结]
本节重点是认识物理变化、化学变化的基本特征;知道物质是由分子、原子等粒子构成的,初步形成物质构成的微粒观;初步树立为民族振兴、为社会进步学习的志向。
[课后作业]
2.完成P6交流共享。
3.记忆有关实验现象。
中考名师初中化学教案【篇3】
教学目标
知识目标
使学生了解,理解放热反应和吸热反应;介绍燃料充分燃烧的条件,培养学生节约能源和保护环境意识;通过学习和查阅资料,使学生了解我国及世界能源储备和开发;通过布置研究性课题,进一步认识化学与生产、科学研究及生活的紧密联系。
能力目标
通过对的学习,培养学生综合运用知识发现问题及解决问题的能力,提高自学能力和创新能力。
情感目标
在人类对能源的需求量越来越大的现在,开发利用新能源具有重要的意义,借此培养学生学会知识的迁移、扩展是很难得的。注意科学开发与保护环境的关系。
教学建议
教材分析
本节是第一章第三节。可以讲是高中化学理论联系实际的开篇,它起着连接初高中化学的纽带作用。本节教学介绍的理论主要用于联系实际,分别从氧化还原反应、离子反应和能量变化等不同反应类型、不同反应过程及实质加以联系和理解,使学生在感性认识中对知识深化和总结,同时提高自身的综合能力。
教法建议
以探究学习为主。教师是组织者、学习上的服务者、探究学习的引导者和问题的提出者。建议教材安排的两个演示实验改为课上的分组实验,内容不多,准备方便。这样做既能充分体现以学生为主体和调动学生探究学习的积极性,又能培养学生的实际操作技能。教师不能用化学课件代替化学实验,学生亲身实验所得实验现象最具说服力。教学思路:影像远古人用火引入课题→→学生实验验证和探讨理论依据→确定吸热反应和放热反应的概念→讨论燃料充分燃烧的条件和保护环境→能源的展望和人类的进步→布置研究学习和自学内容。
课题:
吸热反应和放热反应。
教学难点:
的观点的建立。能量的“储存”和“释放”。
教学过程:
[引入新课]影像:《远古人用火》01/07
[过渡]北京猿人遗址中发现用火后的炭层,表明人类使用能源的历史已非常久远。
一、[板书]
[过渡]化学反应中能量是怎样变化的?
[学生分组实验]请学生注意①操作方法;②仔细观察实验现象;③总结实验结论;④写出化学方程式。
(1)反应产生大量气泡,同时试管温度升高,说明反应过程中有热量放出。化学反应方程式:2Al+6HCl=2AlCl3+3H2↑
(2)混合搅拌后,玻璃片和小烧杯粘在一起,说明该反应吸收了大量的热,使水温降低结成冰。
[结论]
放热反应:化学上把有能量放出的化学反应叫做放热反应。
如CH4(g)+2O2(g)CO2(g)+2H2O(l)
吸热反应:化学上把吸收热量的化学反应叫做吸热反应。
如C(s)+H2O(g)CO(g)+H2(g)
结论:
现代人利用化学反应主要是①利用化学反应中释放出的.能量;②利用化学反应制取或合成新物质。
[板书]二、燃料燃烧的条件和环境保护
[学生分组讨论]
(1)燃料充分燃烧条件?
(2)大量使用化石燃料的缺点?
[结论]
(1)使燃料充分燃烧需要考虑两点:
①燃烧时要有足够多的空气;
②燃料与空气要有足够大的接触面。
空气不足:
①浪费资源;
②产生大量一氧化碳污染空气,危害人体健康。
空气过量:
过量空气会带走部分热量,浪费能源。
增大接触面:
改变燃料的状态。如固体燃料粉碎、将液体燃料以雾状喷出、固体燃料液化等。
(2)大量使用化石燃料:
①能引起温室效应;
②会造成化石燃料蕴藏量的枯竭;
③煤燃烧排放二氧化硫,导致酸雨;
④煤燃烧会产生大量的烟尘。
[板书]三、现代能源结构和新能源展望
结论:人类所需要能量,绝大部分是通过化学反应产生。主要是煤、石油和天然气等化石燃料或它们的制品燃烧所产生的。
中考名师初中化学教案【篇4】
一、教学背景与定位
课型:新授课一课时
学生信息分析:经过一年的化学学习,学生对元素化合物方面的知识有了一定的了解,更重要的是掌握了学习方法,如:实验观察、归纳总结、宏观和微观相结合分析等等。其中实验探究方面的能力还需进一步加强,本单元酸和碱的知识实验较多,且现象比较明显,学生在实验探究方面的能力加强了,很多重要的知识就可以在老师的引导下,通过实验探究的方式加以解决。
教学起点分析:在前两节的学习中,学生已经知道盐酸能与大理石、碱反应,又知道酸溶液中存在H+,能使紫色石蕊试液变红。酸还有哪些性质?如何探究这些性质?这些问题都从学生熟悉的'事物和现象中逐步引出来,由浅入深、循序渐进,符合学生的认知规律。教学过程中应通过学生熟悉的生活实例,如铁锈、水垢等的除去,让学生感知酸的其它化学性质,激发学生对酸的性质探究的兴趣。
二、教学资源与设备
仪器:试管、镊子、药匙、多媒体展示台
药品:浓硫酸、浓盐酸、稀盐酸、镁条、铜丝、木炭、生锈铁钉、氧化铜、碳酸钙、氯化铜溶液、氯化钡溶液
四、教学流程
2、分析酸的化学性质的实质是H+参与反应,总结出酸相似的化学性质。
操作探究
通过蘸有浓硫酸的玻璃棒在空气中的温度变化,让学生设计稀释浓硫酸的方法,理解其原因。
利用多媒体展台,把浓盐酸和浓硫酸的标签进行对比,学生通过交流归纳总结浓硫酸和浓盐酸的主要物理性质;使用浓酸应注意的问题。
活动天地
引入新课
铁制品生锈、水壶底部产生水垢等都是令人讨厌的现象,利用酸的性质,这些问题都可迎刃而解,酸有哪些性质?
练习使用化学用语
实验探究
多识一点
介绍几种其它常见酸如碳酸、硝酸、醋酸、磷酸等的化学式;试总结它们的化学性质。
中考名师初中化学教案【篇5】
教学目标:
1、了解溶解度的涵义和固体溶解度的表示方法
2、了解温度对固体溶解度的影响以及溶解度曲线的意义
3、常识性介绍气体溶解度的表示方法以及温度、压强对气体溶解度的影响关系
固体溶解度的表示方法
教学难点:
1、固体溶解度的表示方法
2、正确认识溶解性与溶解度的表示联系及区别
教学过程:
复习提问:
1、什么叫饱和溶液与不饱和溶液?
2、在饱和溶液的概念中,为什么强调“在一定温度下、一定量的溶剂里”?
引入新课:
【演示一】 20oC时,把蔗糖、食盐分别一份一份地加入10ml水中直到不能溶解为止,
【讨 论】 通过粗略的计算,讨论蔗糖与食盐对水的溶解能力
【提 问】 如果温度不定、溶剂量不同,能否比较他们的溶解能力大小?
【演示二】 20oC时,配制KNO3饱和溶液时有KNO3固体剩余,然后加热,剩余固体又继续溶解
【讨 论】 同一种物质在同一种一定量的溶剂中在不同的温度下,溶解能力是否相同?
【演示三】
1、食盐溶解在水中;
2、食盐放在煤油中;
3、植物油放在水中;
4、植物油放在汽油中
【讨 论】 同一种物质在不同的溶剂里的溶解能力不同
讲授新课:
【板 书】 一、溶解性
1、定义:
2、影响因素:①溶质、溶剂本身的性质(决定性因素)
②外界条件
【过渡】 如何精确地知道一种物质在另一种物质里的溶解性大小是否需要什么条件和标准?
【投影】 列表:20oC时100g水中达到饱和时所溶解的.质量
物质 蔗糖 食盐 硝酸钾 小苏打 熟石灰 大理石
最大质量(g) 203.9 36 31.6 9.6 0.165 0.0013
【讲解】 以上表格中的数据能精确地表示各物质的溶解性大小
二、溶解度
固体溶解度
1、表示方法:
气体溶解度
2、固体溶解度的表示方法:(由表格得)
在一定温度下,固体物质的溶解度通常溶质在100g溶剂
中达到饱和状态时所溶解的质量来表示。
⑴定量表示溶解性大小
⑵理解概念:①一定温度(外界条件)
②100g溶剂(衡量标准)不指明溶剂时为“水”。
③饱和状态:(对溶液的要求)
④溶质的质量:(单位:g)
⑤这种溶质在溶剂里(适用范围)
【提问】 ⑶含义:说出20oC时KNO3的溶解度是31.6g
引申:20oC时KNO3饱和溶液中:
m质:m剂:m液 =S:100g:(S+100g)
=31.6g:100g:131.6g
⑷物质溶解性分类:易溶物质:S > 10g
(室温) 可溶物质:S:1g~10g
微溶物质:S:0.01g~1g
难溶物质:S < 0.01g
巩固:判断投影表格中所属分类
蔗糖、食盐、硝酸钾、小苏打、熟石灰、大理石
师生共同分析P72KNO3在不同温度时的溶解性表
⑸溶解度曲线:
【板书】 画出KNO3的溶解度随温度变化的曲线
或见课本P72几种物质溶解度曲线,
溶解度曲线可表示以下几种关系:
①同一物质在不同温度时的溶解度
②不同物质在同一温度时的溶解度
③物质的溶解度随温度变化而变化的趋势及大小
分析得出变化规律:
A、多数固体物质随温度升高而增大;例如:KNO3,NaNO3等
B、少数固体物质受温度变化影响不大;例如:NaCl
C、极少数固体物质随温度升高而减小;例如:Ca(OH)2
⑹溶解度与溶液的质量分数的区别和联系
区别和联系 溶解度 溶质质量分数
表示方法
计算式
联系
3、气体溶解度的表示方法
⑴定义:某气体在一定温度和一定压强下,溶解在一体积水里达到饱和状态时的体积数
外界条件:温度、压强
⑵影响因素
内部因素:气体与溶剂本身的性质
温度升高,气体溶解度减小
压强不变时
温度降低,气体溶解度增大
压强增大,气体溶解度增大
温度不变时
压强减小,气体溶解度减小
中考点击:
课堂小结:
【投影】
概念
要点
决定因素 定 量 影响
描 述 因素
习 惯 分 类
随堂练习:
教学后记:
上一篇:刚刚2025初中中考化学教案
下一篇:自然界的水化学教案